Descobreix els diferents tipus de mescles en rebosteria i com funcionen per crear textures i sabors únics.

Per Manel Cortés
Les mescles per a rebosteria, també conegudes com a mixes o premezcles, són una solució llesta per utilitzar que conté tots els ingredients necessaris per preparar productes de rebosteria. Aquestes mescles, que solen incloure farina, sucre, llevat i altres ingredients específics, simplifiquen el procés d’elaboració de pastissos, galetes, bescuits i altres dolços.
Aquest número tractarà sobre les diferents mescles, per exemple: dissolució, emulsió, suspensió, mousse (escuma). Ara, vegem una explicació tècnica de cadascuna d’aquestes mescles.
Dissolució
Una dissolució és una mescla homogènia a nivell molecular o iònic de dues o més substàncies, que no reaccionen entre elles, els components de les quals es troben en una proporció que varia dins de certs límits. Primer, la podem descriure de la següent manera: és un sistema en el qual una o més substàncies estan barrejades o dissoltes de manera homogènia en una altra substància. En segon lloc, també es pot definir com una mescla homogènia formada per un dissolvent i per un o diversos soluts.
Un exemple comú podria ser un sòlid dissolt en un líquid, com la sal o el sucre dissolts en aigua; o fins i tot l’or en mercuri, formant una amalgama.
El terme també s’utilitza per fer referència al procés de dissolució. Segons Jöns Jacob Berzelius, la diferència entre solució i dissolució va ser assenyalada per Antoine Lavoisier.
En química, una solució és una mescla homogènia composta d’una sola fase. En una mescla d’aquest tipus, un solut és una substància dissolta en una altra substància, coneguda com a dissolvent. El dissolvent fa possible la dissolució. La solució pren més o menys les característiques del dissolvent, inclosa la seva fase, i el dissolvent és habitualment la fracció principal de la mescla. La concentració d’un solut en una solució és una mesura de la quantitat de solut que es dissol en el dissolvent.
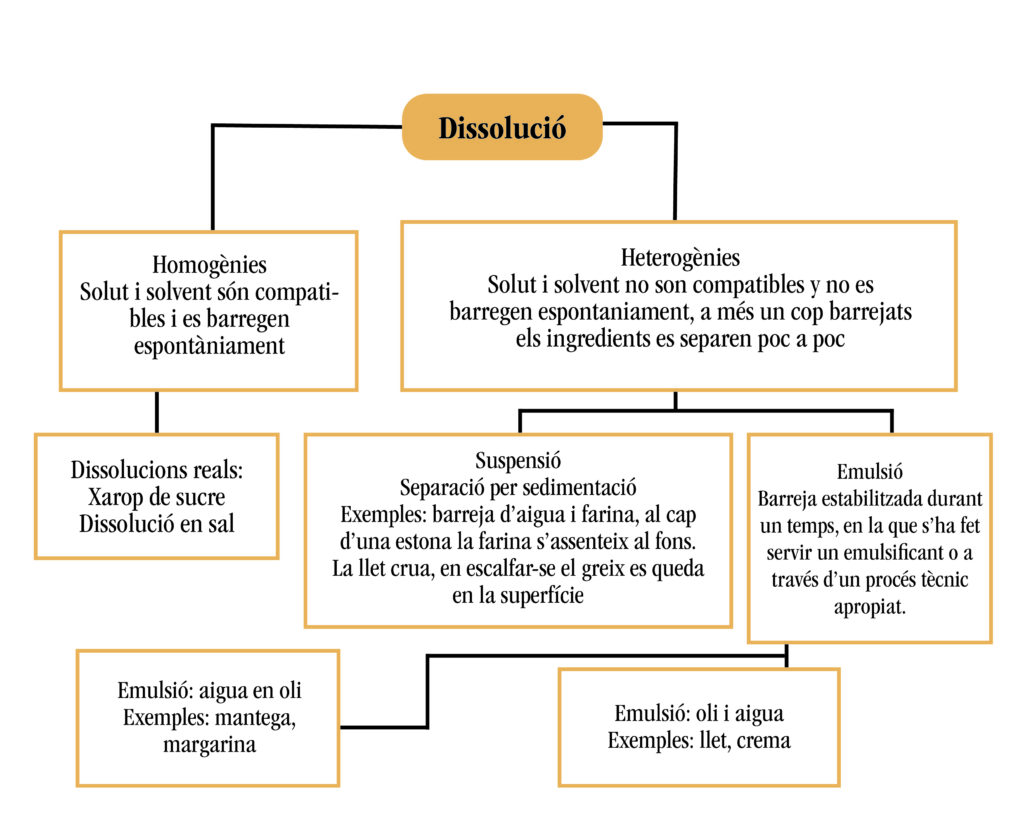
En el treball quotidià, tant a la fleca com a la pastisseria i la confiteria, utilitzem en el nostre receptari fórmules que contenen diferents mescles d’ingredients. D’acord amb les característiques dels components, es barregen amb més o menys facilitat. Mitjançant el coneixement de la manera com les substàncies s’uneixen o es mesclen entre elles, és possible treballar de manera més eficaç i eficient. No sempre és fàcil distingir entre les diverses mescles, sovint les fronteres entre les diferents preparacions no estan clarament definides.
Un cop definit en què consisteix una dissolució, posaré exemples més clars i quotidians. Vegem alguns exemples de dissolucions:
– Dissolució de sucre en aigua = xarop
– Dissolució de sal en aigua = salmorra
– Dissolució d’hidròxid de sodi (sosa càustica) en aigua.
Aquesta es fa servir per a productes com el Brezel alemany, el qual es banya en una dissolució perquè adquireixi aquell color i gust salat tan característic. Per al bany s’utilitza una concentració de sosa càustica d’un màxim entre un 4 i un 4,9% per litre d’aigua.
Concentració d’una dissolució
La solubilitat de l’aigua i el sucre és limitada. Les diferents dissolucions es designen segons el seu grau de saturació, a saber:

Per què es cristal·litza el sucre?
Quan posem aigua i sucre (xarop) en una font de calor, s’escalfen i, a mesura que augmenta la temperatura, l’aigua s’evapora. Així, el grau de saturació (concentració) del xarop augmenta. Quan s’arriba a la concentració desitjada, deixem refredar el xarop, i al cap d’un temps s’observa a la part superior una capa de cristalls de sucre que es van formant. El mateix procés es produeix quan s’ha barrejat (sense escalfar) aigua i sucre i l’aigua s’evapora a temperatura ambient, només que el procés és molt més lent.
Per retardar aquesta acció de cristal·lització, es pot afegir glucosa —entre un 10 i un 30%, segons el tipus de producte— als xarops per tal de retardar la cristal·lització. A més, per aconseguir un efecte encara més gran, es pot afegir crémor tàrtar o àcid tartàric, entre 2 i 3 grams per quilo de sucre.
Vegem una explicació més aclaridora sobre la cristal·lització del sucre:
Quan es dissol el sucre en aigua, les molècules de sucre es desgreguen de la xarxa cristal·lina, però no es descomponen. El dissolvent (aigua), més que destruir la xarxa cristal·lina del sucre, dissocia les molècules de sucre. El nombre depèn de la dissolució de les partícules de solut que entren en contacte amb les partícules lliures del dissolvent (aigua).
Quan la temperatura del dissolvent és alta, les partícules es mouen més de pressa i, per tant, tenen més interaccions amb les partícules de solut (sucre), la qual cosa fa que la velocitat de dissolució de les partícules de la mescla sigui molt més ràpida que en el cas d’una mescla en fred.
Exemple:
A major temperatura, les partícules del solut es dissolen més ràpidament que en estat fred. És per això que, per exemple, una culleradeta de sucre es dissol més de pressa en un cafè calent que en un cafè fred.
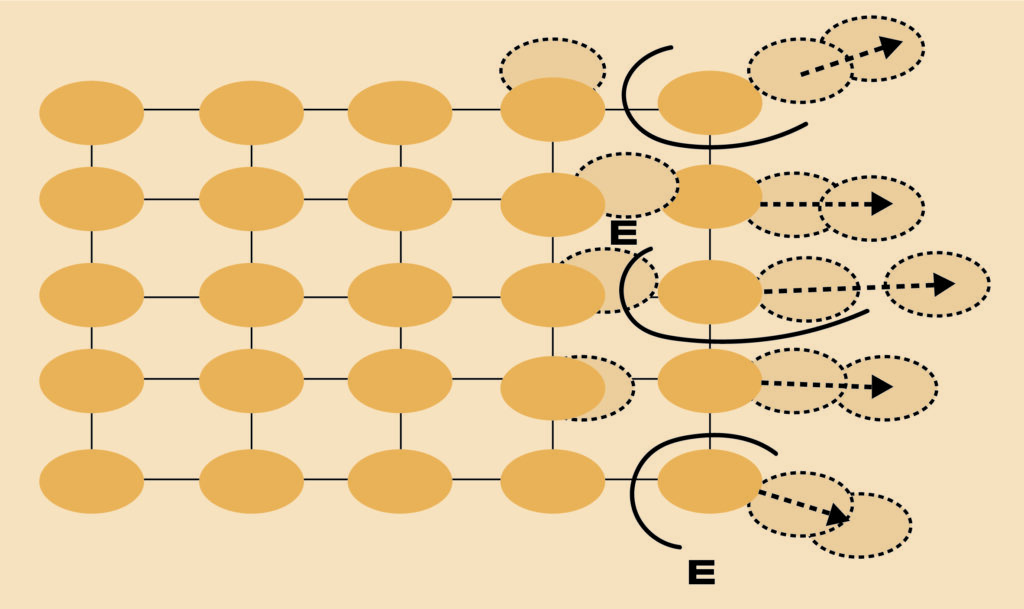
Emulsió
És una mescla de dues substàncies que normalment no es poden barrejar (són immiscibles), ja que, es faci servir la proporció que es faci servir, no formaran una mescla homogènia. Per exemple: l’aigua i l’oli.
Al contrari, es diu que les substàncies són immiscibles si en cap proporció dels seus ingredients són capaces de formar una fase homogènia.
Per aconseguir una emulsió estable, cal afegir-hi un emulsionant per tal d’obtenir una mescla estable i consolidada. Un dels emulsionants més coneguts i utilitzats en pastisseria és l’E-322, lecitina de soja, molt emprat en xocolateria. A la fleca, un dels més usats és l’E-471, mono- i diglicèrids dels àcids grassos.
Què fan els emulsionants?
Són greixos que promouen la formació i estabilització de les emulsions d’aigua i oli:
– Una part anomenada hidòfila (afí a l’aigua)
– Una part anomenada lipòfila (afí al greix o oli)
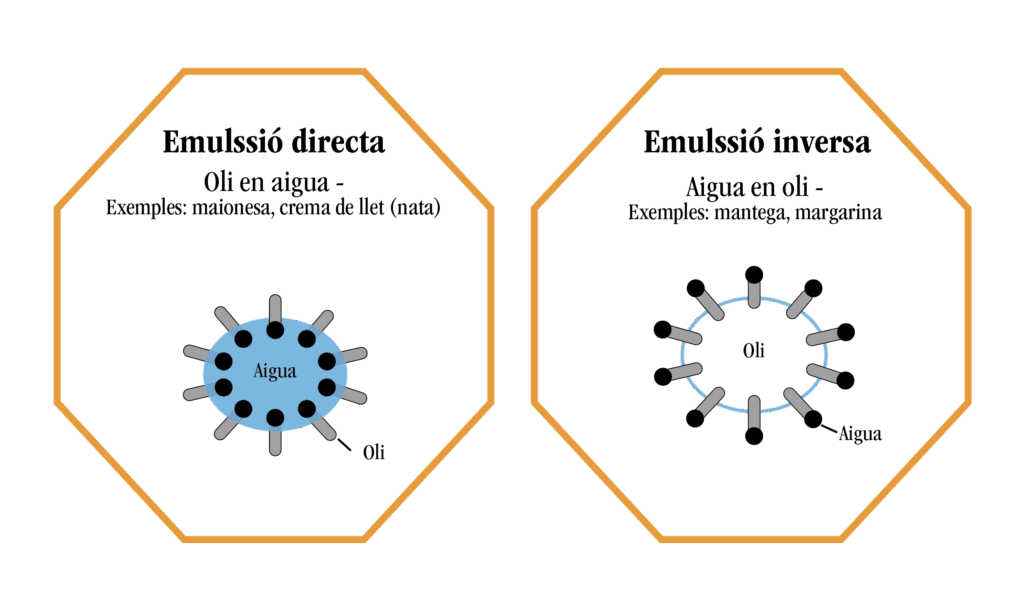
Hi ha dos tipus d’emulsions: una anomenada directa i l’altra anomenada inversa.
Suspensió
La suspensió és una mescla heterogènia formada per un sòlid en pols i/o petites partícules (invisibles a l’ull humà) no solubles (fase dispersa), que es dispersen en un medi líquid (fase dispersant o dispersora). Quan la suspensió reposa, les fases d’una suspensió tendeixen a separar-se, mentre que les d’un col·loide no ho fan.
Exemple: quan barregem llet i midó per espessir una crema, en deixar reposar la mescla, la part sòlida es diposita al fons del recipient.
Col·loide
Els col·loides són mescles intermèdies entre les solucions i les suspensions. Les partícules en els col·loides són més grans que les molècules que formen les solucions.
Parts d’un col·loide
Els col·loides estan formats per dues parts:
1. Fase dispersa o partícules disperses: Aquesta fase correspon al solut en les solucions, i està constituïda per molècules senzilles o molècules gegants com el midó. Poden actuar com a partícules independents o agrupar-se per formar estructures més grans i organitzades.
2. Fase de dispersió o medi dispersant: És la substància en la qual les partícules col·loidals estan distribuïdes. Aquesta fase correspon al dissolvent en les solucions.
La llet és un col·loide: el greix constitueix les partícules disperses i l’aigua és el medi dispersant.
Nota: Si el medi dispersant és l’aigua, hi ha dos tipus de propietats:
– Hidròfobs = repulsió quan el medi és aigua
– Hidrofílics = atracció quan el medi és aigua
Formació de partícules col·loidals
Per a la formació de col·loides s’utilitzen els següents mètodes:
– Dispersió: consisteix a reduir la mida dels ingredients durant el batut o per agitació. Aquests mètodes s’utilitzen per formar emulsions i escumes com la maionesa o la nata muntada.
– El midó i la gelatina es disgreguen espontàniament en partícules col·loidals quan es barregen amb aigua. Escalfant o refredant i batent, s’accelera el procés d’homogeneïtzació.
Per què una mescla per fer un bescuit o un merenga ha d’estar a temperatura ambient o escalfar-se a uns 35 °C ± per obtenir una millor emulsió?
La capacitat coagulant és una qualitat compartida per la clara i el rovell. Abans d’elaborar el batut, hem d’assegurar-nos que els ous (clares o rovells) estiguin a temperatura ambient. Si estan freds, acabats de treure de la nevera, les clares o rovells no muntaran bé. Això passa perquè la incorporació d’aire és molt més lenta per la densitat que provoca el fred en la mescla, ja que les bombolles d’aire necessiten calor per expandir-se correctament durant el batut.
Per què una mescla necessita refredar-se per obtenir una millor homogeneïtzació?
(Per exemple, la nata muntada)
Si la nata té un 35% o més de greix, es pot barrejar amb aire durant el batut, de manera que les bombolles d’aire queden atrapades en una xarxa de gotetes de greix, i el col·loide resultant adquireix aproximadament el doble de volum de la nata original.
Però… si la temperatura de la nata és superior als 10 °C, aquest procés no es produeix adequadament. Amb l’excés de temperatura, el greix es torna més fluid, cosa que fa que l’emulsió no es produeixi, o es retardi molt, agreujant el problema a mesura que la mescla continua escalfant-se.
Importància dels col·loides
1. Tots els teixits vius són col·loïdals.
2. El sòl, en part, està constituït per matèria col·loïdal.
3. Molts dels aliments que ingerim són col·loides: el formatge, la mantega, les sopes clares, les gelees, la maionesa, la nata muntada, la llet.
Tipus de col·loides
Segons l’estat físic en què es trobin la fase dispersa i el medi dispersant, els col·loides prenen diferents noms:
(Si vols, puc continuar amb una taula o classificació segons els estats físics: sòlid, líquid, gas… Només has de dir-m’ho.)
Mousse (escuma)
És una dispersió de gas en un líquid. Un exemple clar i habitual en el nostre sector són les clares d’ou muntades a punt de neu barrejades amb nata muntada (= mousse).
El mousse té una aparença similar a la d’una emulsió, però la diferència principal és que en el mousse s’incorpora un element diferenciador: el gas, com ara l’aire que s’hi introdueix durant el batut. Durant aquesta fase de batut, es formen petites bombolles que creen una xarxa o estructura que dona lloc a la textura lleugera i airejada característica del mousse.
Resumen de las diferentes mezclas









